Lijekovi
Sadržaj Hrvatske farmakopeje
Zašto se HRF više ne tiska kao knjiga?
Zbog brzog razvitka analitičkih tehnika, novih saznanja, npr. O onečišćenjima u djelatnim i pomoćnim tvarima i sl., jako brzo nastaju novi tekstovi i ažuriraju se postojeći tekstovi Ph. Eur. Godišnje Europska farmakopeja objavljuje tri dodatka osnovnom izdanju s novim, ažuriranim ili korigiranim tekstovima, a svake tri godine objavljuje se novo izdanje koje objedinjuje sve dodatke, što je vidljivo samo u tiskanom izdanju Ph. Eur., a u online izdanju vidljivo je uvijek cjelovito izdanje sa svim izmjenama.
Kako se Hrvatska farmakopeja ažurira u skladu s Ph. Eur., to bi značilo učestalo tiskanje novih knjiga i brzo odbacivanje starih izdanja jer je, ne zaboravimo, samo posljednje izdanje važeće. Procijenili smo da bi to značilo velike troškove tiskanja i nepotrebni utrošak velikih količina papira. Osim toga, proces ažuriranja sadržaja u HRF-u bi se tiskanjem dodatno usporio. Kako svi kolege danas rade na računalima, procijenili smo da im online pristup Hrvatskoj farmakopeji ne bi smio biti problem. Pretraživanje elektroničkog izdanja je brže i jednostavnije, a licenca je financijski pristupačnija od tiskanog izdanja.
Kopiranje i tiskanje tekstova Hrvatske farmakopeje je moguće, ali to ne preporučujemo jer nije prema pravilima Dobre dokumentacijske prakse. Napominjemo da je važno prije svakog korištenja farmakopejskog teksta provjeriti je li još uvijek važeći ili je u međuvremenu ažuriran i izvan snage.
Kako da odlučim hoću li nabaviti Ph. Eur. ili HRF? Kako mogu znati koje dijelove Ph. Eur. sadrži HRF?
Kad je riječ o koncepciji HRF-a, možete je pregledati preko demo Hrvatske farmakopeje u koju možete ući preko sljedeće poveznice.
Što se tiče sadržaja prevedenih i neobvezujućih tekstova, možete ih naći u sljedećem popisu.
Ako među prevedenim tekstovima nema teksta koji je vama potreban, pišite nam na adresu UredZaFarmakopeju@halmed.hr i vaše ćemo potrebe nastojati ispuniti u najkraćem mogućem roku.
Je li HRF obvezujući propis ako se stupanje na snagu ne objavljuje preko Narodnih novina?
Prema prijašnjem Zakonu o lijekovima i medicinskim proizvodima (NN, 121/03, 177/04): Čl. 64: "Hrvatsku farmakopeju na prijedlog Agencije donosi ministar nadležan za zdravstvo" (danas HALMED); Čl. 125: "Agencija izrađuje monografije za Hrvatsku farmakopeju".
Prema važećem Zakonu o lijekovima (NN 76/13, 90/14, 100/18): Čl. 21: "Agencija za lijekove i medicinske proizvode: izrađuje Hrvatsku farmakopeju i izdaje Hrvatsku farmakopeju te druge stručne publikacije iz područja svoga rada."
Dakle, od stupanja na snagu posljednjeg Zakona o lijekovima iz 2013. godine Agencija za lijekove i medicinske proizvode objavljuje Hrvatsku farmakopeju, a datumi stupanja na snagu definirani su rezolucijama koje donosi Vijeće Europe i Hrvatska farmakopeja je s njima usklađena
Kako se odabiru monografije za uvrštavanje u HRF?
Hrvatska farmakopeja objavljuje prijevode u Hrvatskoj najčešće korištenih tekstova Europske farmakopeje.
Popis najčešće korištenih tekstova dobiven je velikom anketom svih korisnika u Hrvatskoj. Uz prevedene monografije, prevedeni su i opći članci i reagensi potrebni za izvođenje ispitivanja prema određenoj monografiji, čime je zapravo preveden velik dio općih članaka i općih monografija.
Dosad smo preveli sve tražene tekstove. Zahtjevi za prijevode tekstova monografija se trajno primaju preko predstavnika korisnika u Povjerenstvu za farmakopeju ili na adresu UredZaFarmakopeju@halmed.hr. U svakom izdanju/dodatku HRF-a objavljujemo nove prijevode Ph. Eur. i tako obogaćujemo njegov sadržaj.
Osim obvezujućih tekstova, u HRF-u povremeno objavljujemo i tzv. neobvezujuće tekstove koji bi, prema procjeni Povjerenstva za farmakopeju, mogli biti korisni našim korisnicima. Ti tekstovi objavljuju se zasebno, od poglavlja 15. dalje.
Kako mogu saznati što je novo, revidirano ili ispravljeno u određenom izdanju ili dodatku Ph. Eur.?
U svakom izdanju ili dodatku HRF-a u uvodnom dijelu nalazi se poglavlje u kojem se navode svi novi, revidirani, ispravljeni, uklonjeni tekstovi i tekstovi kojima je izmijenjen naslov, i to u cijeloj Ph. Eur., bez obzira na to je li taj tekst u HRF-u preveden ili nije (popis odgovara Sadržaju odgovarajućeg izdanja ili dodatka Ph. Eur.).
Ako detaljnije želite znati što je izmijenjeno u nekom revidiranom tekstu, podatke možete naći u uvodnom poglavlju Komentari revidiranih tekstova objavljenih u Dodatku x.y Ph. Eur., koje za vas prevodimo za svaki revidirani tekst zasebno iz EDQM-ova online časopisa Pharmeuropa.
Svaki dodatak ili izdanje HRF-a ima Predgovor u kojem su navedeni novoprevedeni tekstovi ili novi tekstovi objavljeni u neobvezujućem dijelu HRF-a te druge novosti vezane uz HALMED-ove i EDQM-ove aktivnosti vezane uz farmakopeju. U samom revidiranom tekstu HRF-a nema posebnih oznaka izmijenjenog teksta.
Svi revidirani ili ispravljeni tekstovi u tiskanom izdanju Europske farmakopeje označeni su okomitim crtama na rubu stranice, a vodoravne crte na rubu stranice ukazuju na područje teksta gdje je dio izbrisan.
U online izdanju Ph. Eur. izmijenjeni dio teksta označen je zelenim strelicama, a brisani tekst simbolom škara.
Kako mogu saznati što je u revidiranoj monografiji izmijenjeno?
Ph. Eur. takve podatke objavljuje na dva načina:
- Odmah nakon revizije u Komentarima revidiranih tekstova objavljenih u Dodatku x.y Ph. Eur., u EDQM-ovu online časopisu Pharmeuropa;
- Isti podaci se nakon toga mogu trajno naći u tzv. Bazi znanja (Knowledge Database) odgovarajuće monografije.
U bazi znanja možete vidjeti i je li neki tekst trenutačno u reviziji, odnosno ako jest, u kojoj je fazi revizije.
Svi revidirani ili ispravljeni tekstovi u tiskanom izdanju Europske farmakopeje označeni su okomitim crtama na rubu stranice, a vodoravne crte na rubu stranice ukazuju na područje teksta gdje je dio izbrisan.
U online izdanju Ph. Eur. izmijenjeni dio teksta označen je zelenim strelicama, a brisani tekst simbolom škara.
U Hrvatskoj farmakopeji možete u izdanju/dodatku u kojem je revizija objavljena naći u uvodnom poglavlju Komentare revidiranih tekstova objavljenih u Dodatku x.y Ph. Eur., koje za vas prevodimo za svaki revidirani tekst zasebno iz EDQM-ova online časopisa Pharmeuropa.
U samom revidiranom tekstu HRF-a nema posebnih oznaka izmijenjenog teksta.
Kako mogu znati koje je izdanje HRF-a važeće?
U pravilu, kod otvaranja aplikacije Hrvatska farmakopeja uvijek vam se otvara važeće izdanje, čiji broj možete vidjeti u zaglavlju.
U ostala izdanja možete ući izbornikom u zaglavlju i birati između Izdanja i Arhiviranih izdanja u kojima se nalaze nešto starija izdanja koja se, u pravilu, manje koriste.
Napominjemo da u zaglavlju možete imati i izdanje koje je objavljeno, ali još nije stupilo na snagu, pa ga morate sami, prema izboru, otvoriti.
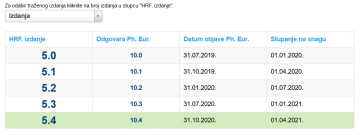
U izborniku u zaglavlju također možete vidjeti kad su pojedina izdanja objavljena, a kad su stupila na snagu.
U navedenom izborniku možete vidjeti koje izdanje HRF-a odgovara kojem izdanju Ph. Eur.
Jesu li svi zahtjevi monografije obvezujući?
U monografiji su neobvezujući sljedeći njezini dijelovi:
- Opis
- Čuvanje
- Označivanje
- Dodatne informacije uz monografiju, u Bazi znanja
- Svojstva povezana s posebnom namjenom - zahtjev je obvezujući pod uvjetima navedenim na početku samog ispitivanja.
Što je to neobvezujući dio farmakopeje?
Neobvezujući dio farmakopeje je onaj koji niste obvezni primjenjivati. On je savjetodavan i informativan.
Ako u poglavlju Opće napomene ili u monografijama nije drugačije navedeno, navodi u monografijama su obvezujući zahtjevi.
Opća poglavlja postaju obvezujuća kad se na njih poziva određena monografija, osim ako citati u tekstu pokazuju da navodi namjerno nisu postavljeni da bi obvezivali, tj. kad se navode samo kao obavijest.
U Ph. Eur. neobvezujući su sljedeći tekstovi:
- Početna poglavlja (predgovor, uvod, popis suradnika) (u HRF-u pod naslovom poglavlja Hrvatska farmakopeja i Europska farmakopeja)
- Tekstovi kojima na samom početku kosim slovima piše da nisu obvezujući, npr. Ovo opće poglavlje nije obvezujuće; ono pruža informacije o…. .
U monografiji su neobvezujući sljedeći njezini dijelovi:
- Opis
- Čuvanje
- Označivanje
- Dodatne informacije uz monografiju, u Bazi znanja
- Svojstva povezana s posebnom namjenom - zahtjev je obvezujući pod uvjetima navedenim na početku samog ispitivanja.
Hrvatska farmakopeja sadrži poglavlja kojih nema u Europskoj farmakopeji. Ona su također neobvezujuća:
- Komentari revidiranih tekstova
- Poglavlje 15 s neobvezujućim tekstovima
- Farmakopejski rječnik
- Rječnik uz poglavlje 5.3.
Kako mogu znati je li neki tekst iz farmakopeje neobvezujući?
Neobvezujući dio farmakopeje je onaj koji niste obvezni primjenjivati. On je savjetodavan, informativan.
Ako u poglavlju Opće napomene ili u monografijama nije drugačije navedeno, navodi u monografijama su obvezujući zahtjevi.
Opća poglavlja postaju obvezujuća kad se na njih poziva određena monografija, osim ako citati u tekstu pokazuju da navodi namjerno nisu postavljeni da bi obvezivali, tj. kad se navode samo kao obavijest.
U Ph. Eur. neobvezujući su sljedeći tekstovi:
- Početna poglavlja (predgovor, uvod, popis suradnika); (u HRF-u pod naslovom poglavlja Hrvatska farmakopeja i Europska farmakopeja)
- Tekstovi kojima na samom početku kosim slovima piše da nisu obvezujući, npr. Ovo opće poglavlje nije obvezujuće; ono pruža informacije o… .
U monografiji su neobvezujući sljedeći njezini dijelovi:
- Opis
- Čuvanje
- Označivanje
- Dodatne informacije uz monografiju, u Bazi znanja
- Svojstva povezana s posebnom namjenom - zahtjev je obvezujući pod uvjetima navedenim na početku samog ispitivanja.
Hrvatska farmakopeja sadrži poglavlja kojih nema u Europskoj farmakopeji. Ona su također neobvezujuća:
- Komentari revidiranih tekstova
- Poglavlje 15 s neobvezujućim tekstovima
- Farmakopejski rječnik
- Rječnik uz poglavlje 5.3.
Je li Rezolucija CM/Res(2016)1 o zahtjevima za osiguranje kakvoće i sigurnosti lijekova izrađenih u ljekarni za posebne potrebe pacijenata obvezujuća, propis?
Ova rezolucija je dokument koji je usvojio Odbor ministara Vijeća Europe, sastavljen isključivo od predstavnika država potpisnica Konvencije o izradi Europske farmakopeje, s ciljem sprečavanja raskoraka u kakvoći i sigurnosti između lijekova izrađenih u ljekarnama i industrijski proizvedenih lijekova te preporučuje da države potpisnice Konvencije o izradi Europske farmakopeje prilagode svoje propise u skladu s načelima izloženima u ovoj rezoluciji.
Kao što vidite, riječ je o preporuci, a ne o obvezi, iako je i Hrvatska zemlja potpisnica Rezolucije, pa bi bilo logično da će je i primijeniti. Ljekarništvo se u EU regulira nacionalnom legislativom, a Vijeće Europe u tom smislu može samo izdati preporuke.
U Hrvatskoj, zasad, nedostaje odgovarajuća zakonska regulativa u području izrade i provjere kakvoće lijekova koji se izrađuju u ljekarnama i njihovih sastavnica.
Ova rezolucija mogla bi u tom smislu u velike pomoći te olakšati i pojednostaviti provjeru kakvoće pripravaka izrađenih u ljekarni. Države koje su implementirale Rezoluciju, uvidjele su sve njezine koristi.
Zašto se uvriježeni tehnički pojmovi prevode na hrvatski jezik?
Jedan od glavnih ciljeva Hrvatske farmakopeje jest očuvanje i razvijanje stručnih farmaceutskih izraza na hrvatskom jeziku.
U Farmakopejskom rječniku je vidljivo da smo nastojali korisnicima ponuditi hrvatske prijevode stručnih naziva. Pritom smo kao izvore koristili brojne stručne rječnike, navedene u literaturi rječnika. Svjesni toga da se neki od izraza nisu ukorijenili u svakodnevnoj uporabi, a ponekad smo koristili i pohrvaćene međunarodne izraze kako ne bi došlo do pogrešnog tumačenja teksta. Tada smo u Farmakopejskom rječniku naveli oba ili više izraza, s time da smo prvome navedenom dali prednost. Napominjemo da za obveznike primjene Europske farmakopeje vrijedi da u slučaju nerazumijevanja teksta ili bilo kakvih sporova trebaju konzultirati tiskano izdanje na jednom od službenih jezika (engleski i francuski jezik).
Ne slažem se s nekim od vaših prijevoda tehničkih izraza. Kome da to napišem?
Za stručna pitanja molimo da kontaktirate Ured za farmakopeju na adresu UredZaFarmakopeju@halmed.hr.
Kako mogu predložiti nove prijevode za HRF?
Prijedlozi za prijevode tekstova monografija se trajno primaju preko predstavnika korisnika u Povjerenstvu za farmakopeju ili izravno na adresu UredZaFarmakopeju@halmed.hr. U svakom izdanju/dodatku HRF-a objavljujemo nove prijevode Ph. Eur. i tako obogaćujemo njegov sadržaj.
Primljeni prijedlog nastojat ćemo što prije prevesti i objaviti u HRF-u.
Što je drugoredna identifikacija?
U Općim napomenama, podnaslov 1.5.1.8 Identifikacija, stoji: "Ispitivanja navedena u ulomku Identifikacija nisu osmišljena tako da daju cjelovit prikaz potvrda kemijske strukture ili sastava proizvoda; ona su namijenjena da daju potvrdu s prihvatljivim stupnjem sigurnosti da je materijal u skladu s opisom na oznaci".
Identifikacijsko ispitivanje može se pozivati na ispitivanje u ulomku monografije Ispitivanja.
Ako monografija navodi, na primjer, identifikacijska ispitivanja A, B i C, sva tri ispitivanja moraju se provesti i moraju udovoljavati zahtjevima.
Pojedine monografije daju dva ili više nizova identifikacijskih ispitivanja koja su ekvivalentna i mogu se koristiti samostalno. Njima prethodi rečenica tipa "Izvedi ispitivanja A, B ili ispitivanja C, D". Na primjer, jednim ispitivanjem se kromatografski određuje enantiomerna čistoća, dok je drugo ispitivanje specifične optičke skretnje; namjena oba niza je ista, tj. provjera je li prisutan ispravni enantiomer.
U nekim je monografijama ulomak Identifikacija podijeljen na sljedeći način:
- Prvoredna identifikacija (eng. first identification): Ispitivanja koja čine prvorednu identifikaciju mogu se koristiti u svim okolnostima.
- Drugoredna identifikacija (eng. second identification): Ispitivanje(a) koje(a) čini(e) drugorednu identifikaciju mogu se koristiti samo u ljekarnama, pod uvjetom da se može dokazati da je materijal u potpunosti sljediv do serije certificirane da udovoljava svim ostalim zahtjevima monografije. Provedba ispitivanja navedenih pod drugorednom identifikacijom je određena nacionalnim propisima.
Napominjemo da se u čl. 17. (4) Pravilnika o normativima i standardima za obavljanje zdravstvene djelatnosti (NN 52/20.) drugoredna identifikacija navodi kao sekundarna: "Osim opreme iz stavka 3. ovoga članka, sukladno opsegu rada, ljekarna mora imati odgovarajuću mogućnost sekundarne identifikacije ulazne sirovine; za izradu pripravaka za oko i drugih sterilnih pripravaka, ljekarna mora imati obveznu aseptičku komoru ili kabinet za rad u čistom s laminarnim strujanjem zraka; za izradu supozitorija i vagitorija, ljekarna mora imati opremu za izradu te ostalu opremu koju zahtijevaju sigurnosno-tehnički listovi sirovina koji se koriste u radu."
Kada moram provesti ispitivanja navedena u ulomku "Svojstva povezana s posebnom namjenom"?
Poglavlje Ph. Eur./HRF 5.15 Svojstva povezana s posebnom namjenom pomoćnih tvari (eng. Functionality-related characteristics of excipients) detaljnije opisuje svrhu ovih ispitivanja.
Ovaj je ulomak uključen u monografiju za informaciju korisniku i nije obvezujući dio monografije. Ulomak daje izjavu o svojstvima za koje se zna da se odnose na određene uporabe pomoćnih tvari. Navedena je uporaba na koju se svojstvo odnosi. Za druge uporabe svojstvo ne mora biti važno. Zbog togaulomak ne treba gledati samo kao dodatak monografiji. Odgovornost je proizvođača lijeka da odluči kako će informaciju o svojstvima povezanima s posebnom namjenom primijeniti u proizvodnom postupku u svjetlu uporabe pomoćne tvari i podataka iz farmaceutskog razvoja.
Dano svojstvo može biti predmet obaveznog zahtjeva u monografiji. Ako je to slučaj za određene uporabe, također je navedeno u ulomku svojstava povezanih s posebnom namjenom, kao mjerodavno svojstvo koje proizvođač lijeka može odabrati da specificira stupanj čistoće korišten u određenom farmaceutskom pripravku.
Namjena je ulomka svojstava povezanih s posebnom namjenom prikazati trenutačno znanje povezano s glavnom uporabom pomoćne tvari. S gledišta višestrukih uporaba nekih pomoćnih tvari te kontinuiranog razvoja novih uporaba, ulomak možda nije potpun. Dodatno, metode navedene za određivanje određenih svojstava dane su kao preporuke za metode poznate kao uspješne za tu namjenu te se ne isključuje uporaba drugih metoda.
Zašto HRF više ne sadrži normirane izraze?
HRF je do dodatka HRF 3.4 objavljivao Normirane izraze u neobvezujućem dijelu farmakopeje.
Naime, dotad je bilo potrebno registrirati se pri EDQM-u i platiti korištenje baze, pa smo na taj način korisnicima HRF-a osiguravali besplatni pristup Bazi normiranih izraza.
Kako je nakon toga EDQM besplatno otvorio pristup bazi Standard Terms (uz prvu registraciju), mi smo prestali objavljivati izraze u HRF-u jer su postali dostupni svim korisnicima.
Ured za farmakopeju je i dalje taj koji prevodi normirane izraze koje je prihvatila Komisija Europske farmakopeje, samo što više ne ažuriramo izraze na dva mjesta, nego samo u izvornoj bazi.
Za pitanja vezana uz Normirane izraze molimo da kontaktirate Ured za farmakopeju na adresu UredZaFarmakopeju@halmed.hr.
Mogu li se tekstovi HRF-a kopirati i tiskati?
Kopiranje i tiskanje tekstova Hrvatske farmakopeje je moguće, ali to ne preporučujemo jer nije prema pravilima Dobre dokumentacijske prakse. Napominjemo da je važno prije svakog korištenja farmakopejskog teksta provjeriti je li još važeći ili je u međuvremenu ažuriran i izvan snage.
Možete li mi poslati samo neku monografiju HRF-a jer mi nije potrebna cijela farmakopeja?
Intelektualna prava na tekstove Europske farmakopeje posjeduje EDQM. EDQM može samo nacionalnim farmakopejama zemalja potpisnica Konvencije o izradi Europske farmakopeje dati prava za korištenje tekstova, a nacionalne farmakopeje ne mogu ih dalje ustupati.
Dakle, HALMED ne šalje korisnicima pojedinačne tekstove Hrvatske farmakopeje.
Iznimka mogu biti neobvezujući tekstovi za koje nismo vezani drugom vrstom ugovora (kao što je Ugovor o suradnji s Britanskom farmakopejom za tekstove Britanske farmakopeje o lijekovima koji ne podliježu odobravanju).
Imam licencu za HRF, ali u njoj nema monografije/teksta Europske farmakopeje koji mi je potreban?
U svakom izdanju/dodatku HRF-a objavljujemo nove prijevode Ph. Eur. i tako obogaćujemo njegov sadržaj. Primljeni zahtjev nastojat ćemo što prije prevesti i objaviti u HRF-u.
Zahtjevi za prijevode tekstova monografija se trajno primaju preko predstavnika korisnika u Povjerenstvu za farmakopeju ili izravno na adresu UredZaFarmakopeju@halmed.hr.
Na koji je način u Hrvatskoj farmakopeji formirano nazivlje biljnih droga?
Radi jednostavnosti pretraživanja, preglednosti i homogenosti izričaja usuglašeno je da nazivlje monografija biljnih droga i biljnih pripravaka, revidirano u Dodatku HRF-a 4.3, ima "indeksirani" oblik po principu nizanja:
"Biljna vrsta, biljni dio, biljni pripravak"
Primjeri indeksiranog oblika naslova monografije
- biljna droga: Anđelika ljekovita, korijen; Sljez crni, cvijet;
- biljni pripravak: Komorač gorki, plod, eterično ulje; Glog, list s cvijetom, suhi ekstrakt.
Nazivi biljnih vrsta za koje nemamo hrvatski prijevod (ili narodni naziv) uglavnom se tvore transkripcijom latinskog naziva biljnog roda (primjerice: "Ginko, list" prema vrsti Ginkgo biloba L. ). Prilikom razmatranja odgovarajućeg naziva, kada je to opravdano, uzela se u obzir ljekarnička tradicija nazivlja biljnih droga.
Usporedo s indeksiranim nazivom navedeni su i u praksi korišteni ljekarnički nazivi biljnih droga (uobičajeno posvojni pridjev izveden od naziva biljne vrste + imenica koja se odnosi na biljni dio; primjerice: Eukaliptusov list, Bazgin cvijet).
Primijenjena pravila pri tvorbi nazivlja monografija biljnih droga i biljnih pripravaka te prisutni izuzeci od tih pravila detaljno su pojašnjeni u uvodnom poglavlju online izdanja HRF-a, odnosno u dijelu "IV. Kako pretraživati" unutar "stabla" "HRVATSKA FARMAKOPEJA".
Mogu li na HALMED-ovim internetskim stranicama pronaći informacije o HRF-u?
Podaci o Hrvatskoj farmakopeji mogu se naći na internetskoj stranici HALMED-a.
Na istoj stranici možete naći poveznice za podatke o Komisiji Europske farmakopeje, nacionalnom farmakopejskom tijelu i Povjerenstvu za farmakopeju.
Također, u tablici možete naći usporedni popis Tekstova Europske farmakopeje i prevedenih tekstova.